PNO - Trong khi Mỹ tạm dừng cấp phép sử dụng với Evusheld, Bộ Y tế cho biết vẫn tiếp tục cho lưu hành thuốc này tại Việt Nam.
| Chia sẻ bài viết: |
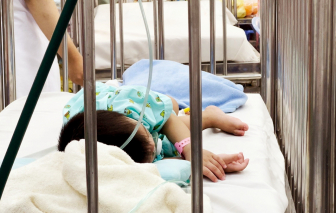
Không ít cha mẹ đau đầu vì đã dùng mọi biện pháp phòng ngừa nhưng trẻ vẫn mắc bệnh tay chân miệng.
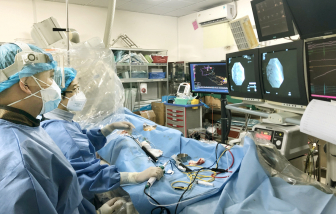
Tại Việt Nam, tỉ lệ mắc rung nhĩ là 1-1,5% dân số. Số ca rung nhĩ mắc mới tăng dần theo độ tuổi, trở thành gánh nặng sức khỏe.

Sau thông tin cơ quan công an triệt phá đường dây sản xuất, buôn bán thuốc giả, Cục Quản lý dược (Bộ Y tế) đã có thêm thông tin về sản phẩm.

Bộ Y tế khẳng định, theo quy định, các thực phẩm không được sử dụng hình ảnh bác sĩ, nhân viên y tế để quảng cáo.

Nhiều phòng khám, bệnh viện tư tại Quảng Ngãi như Bệnh viện Phúc Hưng, phòng khám Thiện Nhân bị Thanh tra Bộ Y tế xử phạt liên quan quảng cáo dịch vụ.

Trong số sản phẩm được Chi cục ATVSTP cấp giấy tiếp nhận bản đăng ký công bố, không có hồ sơ nào có đối tượng dùng là người tiểu đường, suy thận...
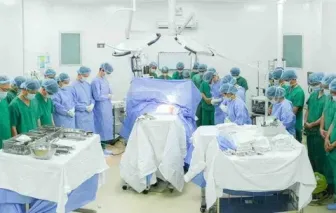
Lần đầu tiên, Bệnh viện Nhân dân 115 đã thực hiện thành công lấy và ghép tạng từ người cho chết não.

Sau 1 năm, bệnh nhân giảm được 40kg, và sau 2,5 năm giảm tổng cộng 67kg, tương đương 50% cân nặng, lấy lại vóc dáng gọn gàng.
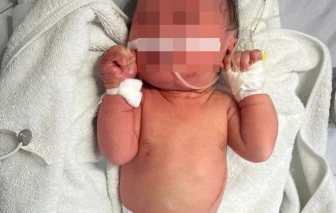
Một bé gái sơ sinh được phát hiện bỏ rơi trong bụi chuối với những vết côn trùng đốt và trầy xước, bầm tím khắp người.
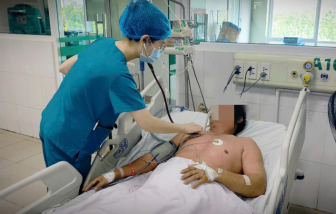
Bộ Y tế thông tin, từ đầu năm tới nay đã có 8 trường hợp tử vong liên quan tới sởi.

Thời gian qua, thông tin gần 600 nhãn hiệu sữa giả được phát hiện khiến nhiều bệnh nhân tiểu đường, suy thận... hoang mang khi chọn sữa.

Điện máy Xanh mang giải pháp lọc nước uy tín đến tận địa phương, giúp bà con chủ động bảo vệ sức khỏe gia đình.
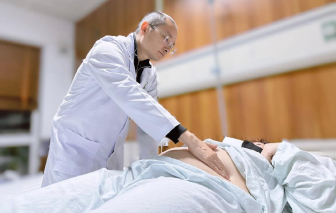
Cô gái 28 tuổi ở Hưng Yên bị kỳ thị ngoại hình dẫn tới trầm cảm nặng nề, thậm chí từng có ý định tự tử.

Sở Y tế tỉnh Đồng Tháp vừa cho biết vẫn chưa đủ căn cứ xác định nguyên nhân gây ngộ độc tại Trường đại học Đồng Tháp khiến 33 người nhập viện.

Cộm mắt kéo dài, ngứa râm ran, người phụ nữ bất ngờ phát hiện có ký sinh trùng dài 10cm ở trong mắt, nguy cơ mù lòa nếu phát hiện muộn.

Cục An toàn thực phẩm đề nghị kiểm tra 2 sản phẩm được quảng cáo như "thần dược chữa bệnh tự kỷ” và “100g sữa bột bằng 20 lít sữa tươi”.

Các vi khuẩn trong miệng có liên quan đến một số tình trạng đau, cho thấy mối quan hệ tiềm ẩn giữa hệ vi sinh vật trong miệng và hệ thần kinh.

Theo Bộ Y tế, mỗi năm có khoảng 40.000 người tự sát tại Việt Nam. Điều đáng lo ngại là trong đó có không ít học sinh, thanh niên.