PNO - Cơ quan Quản lý Thực phẩm và Dược phẩm Mỹ (FDA) cho biết, họ sẽ yêu cầu các chuyên gia bên ngoài cơ quan họp vào cuối tháng 11 để xem xét kỹ lưỡng thuốc viên điều trị COVID-19 của hãng dược Merck.
| Chia sẻ bài viết: |
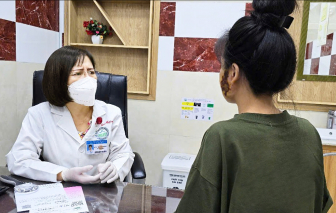
Những ngày qua, Bệnh viện Da liễu TPHCM tiếp nhận nhiều trường hợp bệnh nhân bị phỏng pháo hoa đến điều trị.

Sau 1 tháng sử dụng sản phẩm được quảng cáo “7 ngày giảm 7 cân”, thiếu nữ ở Hà Nội được gia đình phát hiện bất tỉnh, gọi hỏi không đáp ứng.
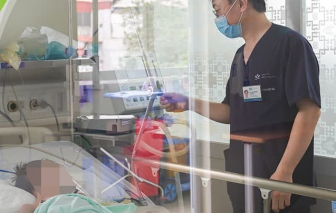
Sau khi bị chó nhà cắn vào vùng mặt, bé trai 7 tuổi (Hà Tĩnh) đã tiêm phòng 3 mũi vắc xin dại nhưng vẫn co giật, yếu tay chân...

Sáng 3/3, Sở Y tế TPHCM cho biết đã thành lập Phòng Bảo vệ, chăm sóc trẻ em và Bảo trợ xã hội.
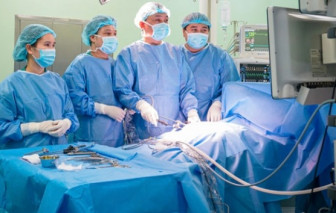
Phương pháp tối ưu để điều trị xoắn ruột ở trẻ em là phẫu thuật nội soi ít xâm lấn.

Những người khỏe mạnh cần uống từ 4 - 6 ly nước lọc mỗi ngày, tùy vào lượng thức ăn và đồ uống khác bạn tiêu thụ.

Một bé sơ sinh 8 ngày tuổi mắc bệnh chuyển hóa hiếm gặp đã được cứu sống thành công.

Kỹ thuật hỗ trợ sinh sản tại Việt Nam đã phát triển vượt bậc, đến nay đã có gần 200.000 trẻ em ra đời bằng phương pháp thụ tinh trong ống nghiệm.

Trẻ sơ sinh và trẻ nhỏ có hệ thống điều hòa thân nhiệt chưa hoàn thiện, nên càng dễ bị ảnh hưởng bởi sự thay đổi nhiệt độ đột ngột này.
Bệnh viện Bạch Mai vừa cảnh báo chiêu trò mạo danh bệnh viện để lừa đảo người đặt lịch khám.

Trên thế giới có hơn 6.000 căn bệnh hiếm được xác định, nhưng đến nay chỉ có khoảng 10% bệnh hiếm có thuốc điều trị.

Sau khi sưng nề vùng hốc mắt, khó thở, buồn nôn, sợ ánh sáng... nữ sinh 15 tuổi được đưa vào viện trong tình trạng nguy kịch, tiên lượng xấu.
Hậu quả của các phương pháp trị nám sai cách khiến da lộ mao mạch, đỏ dễ kích ứng, lão hóa sớm, mất nhiều thời gian tiền bạc để cứu chữa...
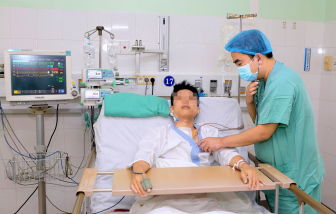
Hơn 23 năm với trên 2.000 ca ghép mô, tạng thành công. Kết quả của Bệnh viện Trung ương Huế có sự đóng góp rất lớn của “đội đặc nhiệm” lấy tạng

Ngày 26/2/2025, Hệ thống Y tế Vinmec vừa được vinh danh “Doanh nghiệp tốt nhất tại Việt Nam”, “Doanh nghiệp vì cộng đồng tốt nhất” và “Nơi làm việc tốt nhất”...

Ngày 27/2, Bộ Y tế phát động “Cuộc thi trắc nghiệm trực tuyến tìm hiểu lịch sử 70 năm ngành y tế Việt Nam”.

20 công trình y học thuộc lĩnh vực y tế thông minh đã được vinh danh tại lễ trao giải thưởng Thành tựu Y khoa Việt Nam năm 2024.

Tối 26/2, Ban Tuyên giáo và Dân vận trung ương, Bộ Y tế phối hợp tổ chức Lễ kỷ niệm 70 năm Ngày Thầy thuốc Việt Nam (27/2/1955-27/2/2025).